Rumus Kimia Asam Karbonat – Asam karbonat adalah asam organik dengan rumus kimia H2CO3. Asam karbonat termasuk asam lemah.
Rumus Kimia Asam Karbonat
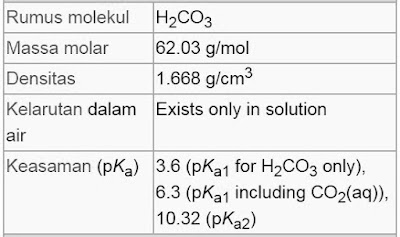
Rumus kimia asam karbonat yakni H2CO3
Keseimbangan Reaksi Kimia Asam Karbonat
Ketika karbon dioksida (CO2) larut dalam air (H2O) maka akan menghasilkan asam karbonat.
CO2 + H2O ⇌ H2CO3. Asam karbonat bisa berubah menjadi ion bikarbonat (HCO3-) dan atom hidrogen.
Peranan Asam Karbonat dalam Darah - Rumus Kimia Asam Karbonat
Asam karbonat merupakan langkah intermediat dalam transpor CO2 ke luar dari tubuh melalui pertukaran gas secara pernapasan. Reaksi hidrasi CO2
umumnya sangat lambat tanpa adanya katalis, tetapi sel darah merah
mengandung enzim karbonik anhidrase, yang dapat meningkatkan laju reaksi
serta mendisosiasi ion hidrogen (H+) dari asam karbonat yang terbentuk, menghasilkan bikarbonat (HCO3-)
yang larut dalam plasma darah. Reaksi yang terkatalisasi ini berbalik
di paru-paru, di mana bikarbonat diubah kembali menjadi CO2
sehingga gas ini dapat dibuang ke luar. Keseimbangan ini berperan
penting sebagai suatu larutan penyangga atau buffer dalam darah mamalia.
Asam karbonat memainkan peran
penting dalam menjaga pH stabil tubuh. PH normal cairan tubuh adalah
sekitar 7,4 dan harus dijaga mendekati nilai ini agar tubuh dapat
berfungsi dengan baik. Jika terjadi perubahan pH, baik naik atau turun,
enzim dapat berhenti berfungsi, otot dan saraf bisa mulai melemah, dan
aktivitas metabolisme menjadi terganggu. Ion bikarbonat dilepaskan dari
asam berfungsi sebagai penyangga yang membantu melawan perubahan pH. Ini
berarti dapat bertindak sebagai asam atau basa saat diperlukan.
Asam didefinisikan sebagai zat yang
melepaskan ion hidrogen menjadi larutan. Basa adalah zat yang menerima
ion hidrogen mereka. Ketika ion hidrogen berlebih menumpuk dalam tubuh,
yaitu cairan menjadi lebih asam, maka ion bikarbonat menerima ion
hidrogen tambahan dan membuat pH tubuh pada tingkat normal. Pada keadaan
terbalik, jika tingkat ion hidrogen turun terlalu banyak, yaitu cairan
menjadi terlalu basa, maka asam karbonat menyerah ion hidrogen untuk
menjaga pH darah normal. Proses ini juga terlihat selama transportasi
oksigen dan karbon dioksida.
Asam karbonat bahkan muncul sebagai
kejadian normal dalam hujan. Saat air hujan jatuh melalui udara,
menyerap karbon dioksida, memproduksi asam karbonat. Dengan demikian,
saat mencapai tanah, ia memiliki pH sekitar 5,5. Hal ini tidak harus
bingung dengan hujan asam yang disebabkan ketika emisi, seperti sulfur
oksida dan nitrogen oksida, dari pembakaran bahan bakar fosil naik ke
udara. Karena jatuh, hujan menyerap komponen ini, menghasilkan asam yang
dapat membuat pH pada hujan menjadi sesedikitnya dua.
Sebagai kesimpulan bahwa rumus kimia asam karbonat yaitu H2CO3.
Demikian yang dapat dibagikan mengenai materi kimia yang telah di ulas
di atas. Penulis berharap ulasan di atas dapat memberikan manfaat yang
baik bagi kita semua terkhusus bagi sahabat para pencinta kimia.




No comments:
Post a Comment