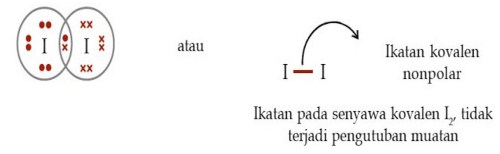
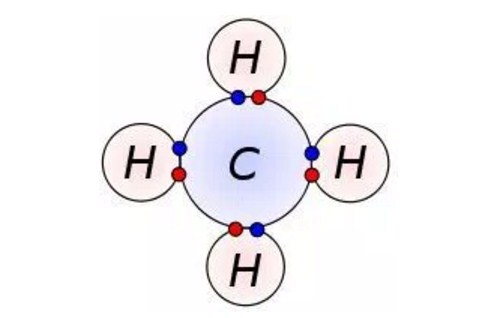
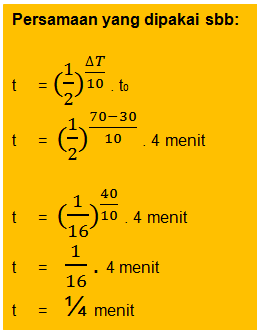1. Tekanan
pada saat uap dan komponen larutan yang tidak menguap dan berada dalam
kesetimbangan disebut...
a. Tekanan uap larutan
b. Tekanan uap jenuh larutan
c. Tekanan parsial
d. Tekanan osmotik
e. Tekanan gas
a. Tekanan uap larutan
b. Tekanan uap jenuh larutan
c. Tekanan parsial
d. Tekanan osmotik
e. Tekanan gas
2. Larutan
yang mengandung 3 gram zat non elektrolit dalam 100 gram air (Kf air =
1,86°C/m) membeku pada suhu -0,279°C. Massa molekul relatif zat tersebut
adalah...
a. 200
b. 95
c. 300
d. 100
e. 132
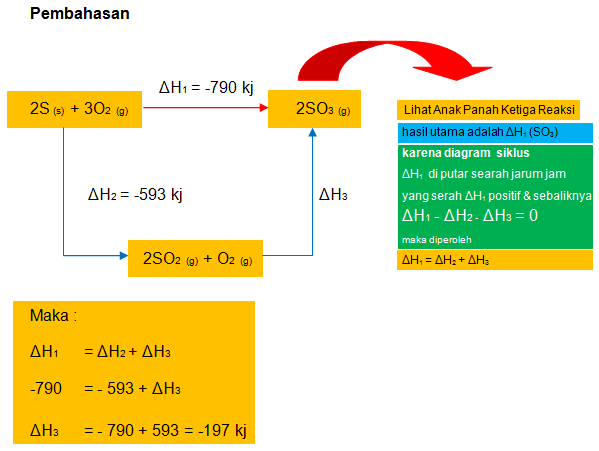
Pembahasan:




Mr = 200
a. 200
b. 95
c. 300
d. 100
e. 132
Pembahasan:
Mr = 200
3. Hasil reaksi untuk elektrolisis
pada larutan  dengan elektrode
Pt adalah...
dengan elektrode
Pt adalah...
a.
b.
c.
d.
e.
Pembahasan:

Anoda :
Katoda :
Reaksi keseluruhan :
a.
b.
c.
d.
e.
Pembahasan:
Anoda :
Katoda :
Reaksi keseluruhan :
4. Sel yang membutuhkan energi
listrik agar reaksi dapat berlangsung adalah...
a. Sel volta
b. Sel elektrolisis
c. Sel galvani
d. Sel elektrokimia
e. Sel kimia
a. Sel volta
b. Sel elektrolisis
c. Sel galvani
d. Sel elektrokimia
e. Sel kimia
5. Unsur gas mulia yang bersifat
radioaktif sehingga sinar yang dipancarkan dapat digunakan dalam terapi kanker
adalah...
a. Xenon
b. Neon
c. Argon
d. Radon
e. Helium
a. Xenon
b. Neon
c. Argon
d. Radon
e. Helium
6. Dibawah ini merupakan kegunaan
senyawa yang mengandung unsur Klorin, kecuali...
a. Sebagai bahan pengawet kayu
b. Sebagai elektrolit pengisi baterai
c. Sebagai pupuk untuk tanaman
d. Sebagai bahan pemutih (bleaching agent)
e. Sebagai pelapis besi
a. Sebagai bahan pengawet kayu
b. Sebagai elektrolit pengisi baterai
c. Sebagai pupuk untuk tanaman
d. Sebagai bahan pemutih (bleaching agent)
e. Sebagai pelapis besi
7. Perhatikan ciri-ciri unsur
dibawah ini :
I. Reaktif bila bereaksi dengan air
II. Mudah mengalami reaksi reduksi
III. Reduktor kuat
IV. Memberikan warna nyala yang khas
Diantara sifat-sifat diatas, yang merupakan sifat unsur alkali adalah...
a. I, II, III
b. II, IV
c. Semua Benar
d. I, III, IV
e. Tidak ada jawaban yang benar
I. Reaktif bila bereaksi dengan air
II. Mudah mengalami reaksi reduksi
III. Reduktor kuat
IV. Memberikan warna nyala yang khas
Diantara sifat-sifat diatas, yang merupakan sifat unsur alkali adalah...
a. I, II, III
b. II, IV
c. Semua Benar
d. I, III, IV
e. Tidak ada jawaban yang benar
8. Proses pembuatan Magnesium dari
air laut yang dicampur dengan CaO sehingga magnesium diendapkan menjadi  adalah...
adalah...
a. Proses Kontak
b. Proses Haber Bosch
c. Proses Downs
d. Proses Gravimetri
e. Proses biokimia
a. Proses Kontak
b. Proses Haber Bosch
c. Proses Downs
d. Proses Gravimetri
e. Proses biokimia
9. Unsur periode ketiga yang
bersifat metaloid adalah...
a. Natrium
b. Silika
c. Klorin
d. Magnesium
e. Argon
a. Natrium
b. Silika
c. Klorin
d. Magnesium
e. Argon
10. Pasangan hidroksida yang
bersifat asam adalah...
a.
b. c.
c. 
d.
e. NaOH dan NaCl
a.
b.
d.
e. NaOH dan NaCl
11. Alasan yang tepat terhadap
kemampuan unsur transisi periode keempat dapat membentuk senyawa dengan warna yang khas adalah..
a. Karena unsur tersebut merupakan unsur logam
b. Karena subkulit 3d tidak terisi penuh
c. Karena ikatan unsur transisi dengan unsur lain sangat kuat
d. Tidak ada jawaban yang tepat
e. Karena unsur tersebut merupakan unsur amfoter
a. Karena unsur tersebut merupakan unsur logam
b. Karena subkulit 3d tidak terisi penuh
c. Karena ikatan unsur transisi dengan unsur lain sangat kuat
d. Tidak ada jawaban yang tepat
e. Karena unsur tersebut merupakan unsur amfoter
12. Logam transisi yang
keberadaannya paling melimpah di alam adalah...
a. Mangan
b. Nikel
c. Zink
d. Ferrum
e. Platina
a. Mangan
b. Nikel
c. Zink
d. Ferrum
e. Platina
13. Reaksi penggabungan inti-inti
atom ringan menjadi inti atom yang lebih berat dinamakan reaksi...
a. Reaksi fusi
b. Reaksi fisi
c. Reaksi subtitusi
d. Reaksi adisi
e. Reaksi eliminasi
a. Reaksi fusi
b. Reaksi fisi
c. Reaksi subtitusi
d. Reaksi adisi
e. Reaksi eliminasi
14. Unsur  meluruh hingga tersisa 25% selama 2 minggu.
Waktu paruh untuk unsur tersebut adalah...
meluruh hingga tersisa 25% selama 2 minggu.
Waktu paruh untuk unsur tersebut adalah...
a. 14 hari
b. 7 hari
c. 28 hari
d. 2 minggu
e. 21 hari
Pembahasan:
No = 100 %
Nt = 25 %
t = 14 hari
a. 14 hari
b. 7 hari
c. 28 hari
d. 2 minggu
e. 21 hari
Pembahasan:
No = 100 %
Nt = 25 %
t = 14 hari
t 1/2 = 7 hari
15. Reaksi alkohol dengan asam
karboksilat disebut dengan reaksi...
a. Saponifikasi
b. Hidrasi
c. Esterifikasi
d. Eliminasi
e. Transformasi
a. Saponifikasi
b. Hidrasi
c. Esterifikasi
d. Eliminasi
e. Transformasi
16. Oksidasi alkohol primer dengan
aldehida menggunakan oksidator dan dalam lingkungan asam dapat menghasilkan
senyawa...
a. Keton
b. Ester
c. Asam alkanoat
d. Eter
e. Alkil alkanoat
a. Keton
b. Ester
c. Asam alkanoat
d. Eter
e. Alkil alkanoat
17.
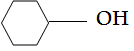
Nama IUPAC untuk senyawa dengan gugus OH seperti di atas adalah...
a. Metilbenzena
b. Hidroksibenzena
c. Toluena
d. Metoksibenzena
e. Fenol

Nama IUPAC untuk senyawa dengan gugus OH seperti di atas adalah...
a. Metilbenzena
b. Hidroksibenzena
c. Toluena
d. Metoksibenzena
e. Fenol
18. Dihaloalkana dapat disintesis
dengan cara mengadisi alkena dengan senyawa...
a.
b. HX
c. MxXy
d. XxOy
e. XO
a.
b. HX
c. MxXy
d. XxOy
e. XO
19. PVC (Polivinil Klorida)
merupakan polimer yang terbentuk melalui proses polimerisasi adisi dari
monomer...
a. Kloroetana
b. Viniletana
c. Polietana
d. Polikloro etana
e. Floroetana
a. Kloroetana
b. Viniletana
c. Polietana
d. Polikloro etana
e. Floroetana
20. Uji biuret yang merupakan uji
bagi zat yang mengandung ikatan peptida. Uji ini positif jika hasil pengujian
menunjukkan...
a. Warna merah bata
b. Warna biru
c. Warna ungu
d. Warna hitam
e. Warna jingga
a. Warna merah bata
b. Warna biru
c. Warna ungu
d. Warna hitam
e. Warna jingga