Wednesday, November 30, 2016
Trik Mencari ΔH Reaksi Jika Soal Berupa Diagram Siklus
Mencari ΔH Jika Soal Berupa Diagram Siklus dengan sangat mudah
Contoh Soal
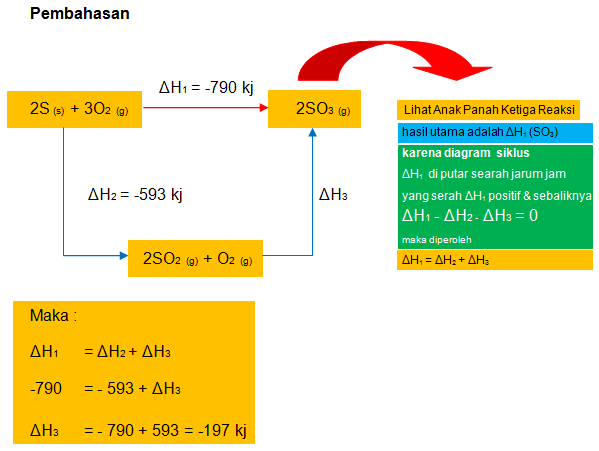
Perhatikan diagram siklus berikut ini
 Dari diagram diatas , harga ΔH3 adalah
Dari diagram diatas , harga ΔH3 adalah
A. – 197 kj
B. + 197 kj
C. – 1383 kj
D. + 1383 kj
E. – 1970 kj

semoga dapat bermanfaat bagi semua ....
Contoh Soal
Perhatikan diagram siklus berikut ini

A. – 197 kj
B. + 197 kj
C. – 1383 kj
D. + 1383 kj
E. – 1970 kj


semoga dapat bermanfaat bagi semua ....
Monday, November 28, 2016
Menghitung Titik Didih Larutan
Contoh Soal
Sebanyak 4 gram NaOH Mr 40 dilarutkan dalam 750 gram air. Jika derajat ionisasi larutan NaOH 75% dan Kf air 1,86, maka penurunan titik beku larutan NaOH adalah....
A. - 0,45 0C
B. – 0,25 0C
C. 0,25 0C
D. 0,45 0C
E. 0,75 0C

Contoh Soal
Sebanyak 45 gram senyawa dengan rumus molekul (H2CO)x dilarutkan dalam 500 gram air ( Kf = 1,86 der/m) . jika titik beku senyawa ini – 0,93 0C dan Ar C = 12 H = 1 O = 16 maka harga x adalah...
A. 12
B. 10
C. 8
D. 6
E. 4

Semoga Bermanfaat
Sebanyak 4 gram NaOH Mr 40 dilarutkan dalam 750 gram air. Jika derajat ionisasi larutan NaOH 75% dan Kf air 1,86, maka penurunan titik beku larutan NaOH adalah....
A. - 0,45 0C
B. – 0,25 0C
C. 0,25 0C
D. 0,45 0C
E. 0,75 0C

Contoh Soal
Sebanyak 45 gram senyawa dengan rumus molekul (H2CO)x dilarutkan dalam 500 gram air ( Kf = 1,86 der/m) . jika titik beku senyawa ini – 0,93 0C dan Ar C = 12 H = 1 O = 16 maka harga x adalah...
A. 12
B. 10
C. 8
D. 6
E. 4

Semoga Bermanfaat
Cara Mudah Menentukan Menentukan Reaksi Elektrolisis
Contoh Soal
Tuliskan Reaksi Elektrolisis larutan dengan elektroda C
1. Larutan MgCl2
2. Leburan/Lelehan MgCl2

Tuliskan Reaksi Elektrolisis larutan dengan elektroda C
1. Larutan MgCl2
2. Leburan/Lelehan MgCl2

Catatan:
Reaksi pada Katoda
Jika
yang menuju katoda adalah ion posistif golongan IA, IIA, Al, dan Mn maka
berlaku
Bila
berupa larutan:
Ion-ion ini tidak
tereduksi, yang tereduksi adalah pelarutnya, air/H2O karena E0
reduksi lebih besar: reaksi sbb:
2H2O + 2e
→ 2OH- + H2
Bila
berupa leburan
Ion tersebut yang akan
tereduksi
Reaksi pada Anoda
Jika
anodanya inert/tak akktif seperti Pt, Au, C
Bila
anion F, Cl, Br, I maka yang terokdidasi:
2F- → F2+ 2e
Trik menghitung potensial sel
Cara Mudah menghitung Potensial Sel dengan sangat cepat
 Contoh Soal 1
Contoh Soal 1
Jika diketahui :
Mg + 2Ag+ → Mg2+ + 2Ag E0 = +3,12 V
Ag+ + e → Ag E0 = +0,80 V
Cu2+ + 2e → Cu E0 = +0,34 V
Maka potensial standar untuk reaksi berikut adalah....
Mg + Cu2+ → Mg2+ + Cu

Contoh Soal 2
Diketahui potensial reduksi standar sbb:
Fe3+ / Fe2+ = +0,77 V
Cu2+ / Cu = +0,34 V
Zn2+ / Zn = -0,76 V
Mg2+ / Mg = -2,37 V
Untuk Reaksi
Mg + 2Fe3+ → Mg2+ + 2Fe2+ memiliki potensial sel ..

Semoga Bermanfaat.....
 Contoh Soal 1
Contoh Soal 1Jika diketahui :
Mg + 2Ag+ → Mg2+ + 2Ag E0 = +3,12 V
Ag+ + e → Ag E0 = +0,80 V
Cu2+ + 2e → Cu E0 = +0,34 V
Maka potensial standar untuk reaksi berikut adalah....
Mg + Cu2+ → Mg2+ + Cu

Diketahui potensial reduksi standar sbb:
Fe3+ / Fe2+ = +0,77 V
Cu2+ / Cu = +0,34 V
Zn2+ / Zn = -0,76 V
Mg2+ / Mg = -2,37 V
Untuk Reaksi
Mg + 2Fe3+ → Mg2+ + 2Fe2+ memiliki potensial sel ..

Semoga Bermanfaat.....
Trik Menghitung Laju Reaksi Kimia Dengan Mudah dan Sangat Cepat
Coba kita lihat contoh berikut ini:
Contoh Soal
Tiap
Kenaikan 100 C laju reaksi suatu zat akan naik dua kali semula.
Jika pada suhu 300 C reaksi tersebut berlangsung selama 4 menit ,
maka pada suhu 700C reaksi tersebut akan berlangsung selama....
A.
¼ menit
B.
½ menit
C.
1 menit
D.
2 menit
E.
4 menit
Pembahasan
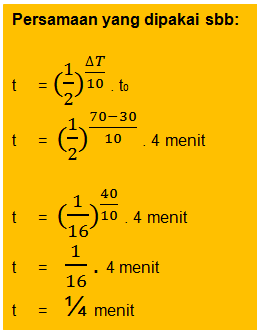
Dengan Rumus diatas Kita kesulitan menghafal persamaannya
Tapi Trik Berikut Kita tidak perlu hafal rumusnya
Berikut ada Trik Cepat dan Mudahnya

Sunday, November 27, 2016
Ikatan Kovalen (Polar dan nonPolar) Beserta Contoh Ikatannya
Ikatan Kovalen - Selain ikatan ion, terdapat juga ikatan kovalen
yang memiliki pengertian adalah ikatan kimia yang terjadi jika adanya
penggunaan pasangan elektron secara bersama-sama oleh atom-atom yang
berikatan. Dengan kata lain, pasangan elektron ini digunakan
bersama-sama (shared electron / elektron sekutu). Sebagai contoh
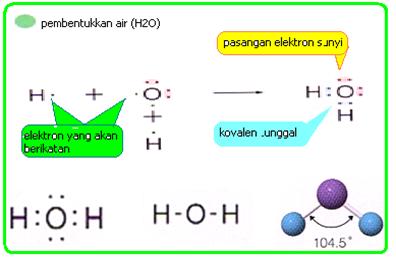
sederhana adalah adanya ikatan kovalen yang terjadi antara unsur
hidrogen dengan oksigen membentuk air (H2O). Masing-masing
ikatan kovalen mengandung dua elektron, yaitu satu berasal dari hidrogen
dan satunya lagi berasal dari oksigen.
Atom berikatan kovalen dengan atom
lain untuk mencapai kestabilan. Dengan adanya "penyekutuan" elektron
valensi, atom dapat memenuhi orbital atom terluarnya dan mencapai
kestabilan.
Jenis-jenis Ikatan Kovalen
Ada dua macam ikatan kovalen, yaitu
ikatan kovalen polar dan non polar. Perbedaan di antara keduanya adalah
asal pemakaian elektron yang digunakan untuk berikatan. Berikut adalah
perbedaan ikatan kovalen polar dan nonpolar.
1. Ikatan Kovalen Polar
Ikatan kovalen polar adalah ikatan
kovalen yang terbentuk ketika elektron sekutu di antara atom tidak
benar-benar dipakai bersama. Hal ini terjadi ketika satu atom mempunyai
elektronegativitas yang lebih tinggi daripada atom yang lainnya. Atom
yang mempunyai elektronegativitas yang tinggi mempunyai tarikan elektron
yang lebih kuat. Akibatnya elektron sekutu akan lebih dekat ke atom
yang mempunyai elektronegativitas tinggi.
Dengan kata lain, akan menjauhi atom
yang mempunyai elektronegativitas rendah. Ikatan kovalen polar
menjadikan molekul yang terbentuk mempunyai potensial elektrostatis.
Potensial ini akan membuat molekul lebih polar, karena ikatan yang
terbentuk dengan molekul polar lain relatif lemah. Ilustrasi ikatan
kovalen polar seperti contoh berikut ini:
Contoh ikatan kovalen polar
Dalam pembentukan molekul HF, kedua elektron dalam ikatan kovalen
digunakan tidak seimbang oleh inti atom H dan inti atom F sehingga
terjadi pengutuban atau polarisasi muatan.
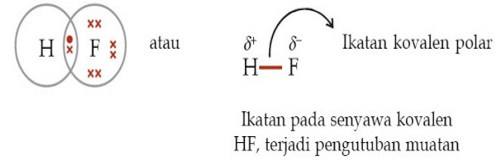
Contoh senyawa kovalen polar adalah NH3,PCl3, H2O, dan Cl2O. Perhatikan struktur Lewis untuk senyawa PCl3 dan H2O berikut:
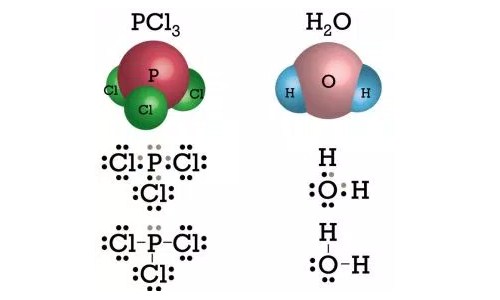
2. Ikatan Kovalen Non Polar
Ikatan kovalen nonpolar adalah
ikatan kovalen yang terbentuk ketika atom membagikan elektronnya secara
setara (sama). Biasanya terjadi ketika ada atom mempunyai afinitas
elektron yang sama atau hampir sama. Semakin dekat nilai afinitas
elektron, maka semakin kuat ikatannya.
Ikatan kovalen nonpolar terjadi pada
molekul gas, atau yang sering disebut sebagai molekul diatomik. Ikatan
kovalen nonpolar mempunyai konsep yang sama dengan ikatan kovalen polar,
yaitu atom yang mempunyai nilai elekronegativitas tinggi akan menarik
elektron lebih kuat. Pernyataan tesebut benar, namun jika terjadi pada
molekul diatom (dimana atom penyusunnya adalah sama) maka
elektronegativitas juga sama. Ilustrasi ikatan kovalen nonpolar seperti
contoh berikut ini:
Contoh Ikatan Kovalen non Polar
Misalnya pada Iodine (I). Dalam pembentukan molekul I2, kedua
elektron dalam ikatan kovalen digunakan secara seimbang oleh kedua inti
atom iodin tersebut. Oleh karena itu, tidak akan terbentuk muatan
(tidak terjadi pengutuban atau polarisasi muatan).
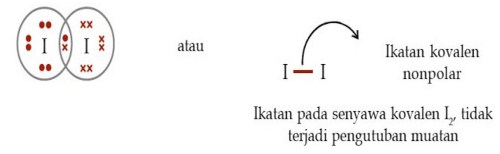
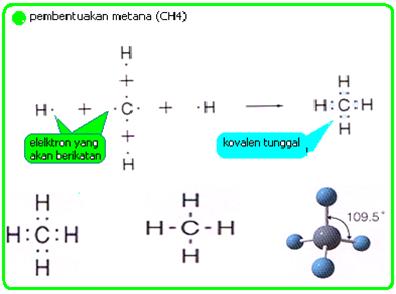
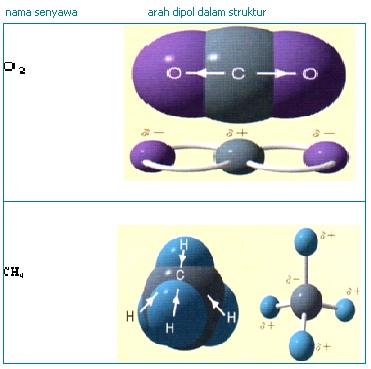
Contoh senyawa lain yang memiliki bentuk molekul simetris dan bersifat nonpolar adalah CH4, BH3, BCl3, PCl5, dan CO2. Perhatikan struktur salah satu ikatan kovalen non Polar dari CH4 berikut:
Rumus dan Contoh Soal Tekanan Osmotik Larutan Elektrolit
Rumus dan Contoh Soal Tekanan Osmotik Larutan Elektrolit
- Dalam materi sifat koligatif larutan elektrolit, selain penurunan
tekanan uap jenuh serta kenaikan titik didih dan penurunan titik didih,
juga dikenal tekanan osmotik larutan elektrolit.
 |
| Rumus dan Contoh Soal Tekanan Osmotik Larutan Elektrolit |
Rumus dan Contoh Soal Tekanan Osmotik Larutan Elektrolit
Pada kesempatan ini RumusKimia.net akan membahas materi khusus Rumus dan Contoh Soal Tekanan Osmotik Larutan Elektrolit.
Untuk mengetahui tekanan osmotik melalui persamaan atau rumus yang
berlaku, tetap dihubungkan dengan faktor van't Hoff. Tekanan osmotik
untuk larutan elektrolit diturunkan dengan mengalikan faktor van't Hoff
[lihat Sifat Koligatif Larutan Elektrolit]. Berikut persamaannya:
π = MRT {1 + (n – 1) α }
Keterangan:
- π = Tekanan osmotik (atm)
- R = Tetapan Gas (0,082 L atm/mol K)
- T = Suhu absolut larutan (K)
- M = molaritas larutan (mol/L)]
- n = jumlah ion dari elektrolit
- α = derajat ionisasi elektrolit
Catatan:
- Jika diketahui suhu bukan dalam derajat Kelvin, maka di ubah satuannya menjadi derajat Kelvin.
- Untuk penentuan [M = molaritas larutan (mol/L)] digunakan persamaan:

[Untuk lebih jelasnya mengenai Molaritas, Lihat Perhitungan Molalitas]
Perhatikanlah contoh-contoh soal berikut ini:
Contoh Soal 1
Sebanyak 5,85 gram NaCl (Mr = 58,5
g/mol) dilarutkan dalam air sampai volume 500 mL. Hitunglah tekanan
osmotik larutan yang terbentuk jika diukur pada suhu 27 °C dan R = 0,082
L atm/mol K.
Jawab:
diketahui, NaCl (n = 2) dan α = 1
π = MRT {1 + (n – 1)α }

= 9,84 atm
Jadi, tekanan osmotik larutan tersebut adalah 9,84 atm.
Contoh Soal 2
Sebanyak 38 g elektrolit biner (Mr =
95 g/mol) dilarutkan dalam air sampai dengan volume 1 L pada suhu 27 °C
dan memiliki tekanan osmotik 10 atm. Hitunglah derajat ionisasi
elektrolit biner tersebut.
Jawab:
π = M R T {1 + (n – 1)α }
α = 0,016
Jadi, derajat ionisasi larutan tersebut adalah 0,016.
Contoh Soal Pilihan Ganda Analisis
Jika diketahui tekanan osmotik larutan 10 gram asam benzoat, C6H5COOH, dalam benzena adalah 2 atm pada suhu tertentu, larutan 20 gram senyawa binernya (C6H5COOH)2 dalam pelarut yang sama memiliki tekanan osmotik sebesar....
A. 0,5 atm
B. 1,0 atm
C. 2,0 atm
D. 4,0 atm
E. 8,0 atmPembahasan:
Oleh karena perbandingan massa / Mr sama, molaritas akan sama dan tekanan osmotik pun sama. Jadi, tekanan osmotiknya sebesar (A) 2 atm.
Nach demikian share materi kimia kali ini mengenai Rumus dan Contoh Soal Tekanan Osmotik Larutan Elektrolit.
Semoga materi kimia di atas dapat memberikan manfaat bagi kita semua.
Mohon saran dari sahabat dalam pengembangan materi kimia kali ini dan
selanjutnya.
Sunday, November 13, 2016
BUKU SMA KELAS 10 Kurikulum 2013 Revisi 2018
BUKU SMA KELAS 10 Kurikulum 2013 Revisi 2016
BUKU Kurikulum 2013 SMA KELAS 10 Revisi 2016
Buku Guru
Kelas 10 SMA Pendidikan Jasmani Olahraga & Kesehatan Guru 2016
Kelas 10 SMA Sejarah Indonesia Guru 2016
BUKU SMA KELAS 10 Kurikulum 2013 Revisi 2016
BUKU Kurikulum 2013 SMA KELAS 10 Revisi 2016
Kelas 10 SMA Pendidikan Jasmani Olahraga & Kesehatan Guru 2016:
Kelas 10 SMA Sejarah Indonesia Guru 2016:
1. Download Buku Guru ( DOWNLOAD)
Kelas 10 SMA Bahasa Indonesia Guru 2016
Kelas 10 SMA Bahasa Inggris Guru 2016
Kelas 10 SMA Pendidikan Pancasila & Kewarganegaraan Guru 2016
Kelas 10 SMA Pendidikan Agama Islam dan Budi Pekerti Guru 2016
Kelas 10 SMA Matematika Guru 2016
Kelas 10 SMA Bahasa Inggris Siswa 2016
Kelas 10 SMA Matematika Siswa 2016
Kelas 10 SMA Pendidikan Jasmani Olahraga & Kesehatan Siswa 2016
Kelas 10 SMA Pendidikan Agama Islam dan Budi Pekerti Siswa 2016
Kelas 10 SMA Pendidikan Pancasila & Kewarganegaraan Siswa 2016
Kelas 10 SMA Bahasa Indonesia Siswa 2016
Kelas 10 SMA Sejarah Indonesia Semester 2 Siswa 2016
Kelas 10 SMA Sejarah Indonesia Semester 1 Siswa 2016
BUKU Kurikulum 2013 SMA KELAS 10 Revisi 2014
Kelas 10 SMA Pendidikan Agama Katolik dan Budi Pekerti Guru
Kelas 10 SMA Pendidikan Agama Hindu dan Budi Pekerti Guru
Kelas 10 SMA Pendidikan Agama Konghuchu dan Budi Pekerti Guru
Kelas 10 SMA Bahasa Indonesia Guru
Kelas 10 SMA Pendidikan Agama Buddha dan Budi Pekerti Guru
Kelas 10 SMA Prakarya dan Kewirausahaan Guru
Kelas 10 SMA Sejarah Indonesia Guru
Kelas 10 SMA Pendidikan Agama Kristen dan Budi Pekerti Guru
Kelas 10 SMA Matematika Guru
Kelas 10 SMA Pendidikan Agama Islam dan Budi Pekerti Guru
Kelas 10 SMA Penjaskes Guru
Kelas 10 SMA Bahasa Inggris Guru
Kelas 10 SMA Sejarah Indonesia Siswa
Kelas 10 SMA Bahasa Indonesia Siswa
Kelas 10 SMA Seni Budaya Siswa
Kelas 10 SMA Prakarya dan Kewirausahaan Siswa
Kelas 10 SMA Matematika Siswa Semester 1
Kelas 10 SMA Matematika Siswa Semester 2
Kelas 10 SMA Pendidikan Agama Konghuchu dan Budi Pekerti Siswa
Kelas 10 SMA Pendidikan Agama Katolik dan Budi Pekerti Siswa
Kelas 10 SMA Penjaskes Siswa
Kelas 10 SMA Bahasa Inggris Siswa
Kelas 10 SMA Pendidikan Agama Islam dan Budi Pekerti Siswa
Kelas 10 SMA Pendidikan Agama Buddha dan Budi Pekerti Siswa
Kelas 10 SMA Pendidikan Agama Hindu dan Budi Pekerti Siswa
BUKU Kurikulum 2013 SMA KELAS 10 Revisi 2016
Buku Guru
Kelas 10 SMA Pendidikan Jasmani Olahraga & Kesehatan Guru 2016:
2. Download Buku Siswa ( DOWNLOAD)
1. Download Buku Guru ( DOWNLOAD)
2. Download Buku Siswa Semester 1 ( DOWNLOAD)
3. Download Buku Siswa Semester 2 ( DOWNLOAD)
Kelas 10 SMA Bahasa Indonesia Guru 2016
Kelas 10 SMA Bahasa Inggris Guru 2016
Kelas 10 SMA Pendidikan Pancasila & Kewarganegaraan Guru 2016
Kelas 10 SMA Pendidikan Agama Islam dan Budi Pekerti Guru 2016
Kelas 10 SMA Matematika Guru 2016
Buku Siswa
Kelas 10 SMA Bahasa Inggris Siswa 2016
Kelas 10 SMA Matematika Siswa 2016
Kelas 10 SMA Pendidikan Jasmani Olahraga & Kesehatan Siswa 2016
Kelas 10 SMA Pendidikan Agama Islam dan Budi Pekerti Siswa 2016
Kelas 10 SMA Pendidikan Pancasila & Kewarganegaraan Siswa 2016
Kelas 10 SMA Bahasa Indonesia Siswa 2016
Kelas 10 SMA Sejarah Indonesia Semester 2 Siswa 2016
Kelas 10 SMA Sejarah Indonesia Semester 1 Siswa 2016
BUKU Kurikulum 2013 SMA KELAS 10 Revisi 2014
Buku Kurikulum 2013-Kurikulum Nasional SMA Semester 1-2 Kelas 10
Links Download Buku Kurikulum 2013-Kurikulum Nasional SMA Semester 1-2 Kelas 10Buku Guru
Kelas 10 SMA Seni Budaya GuruKelas 10 SMA Pendidikan Agama Katolik dan Budi Pekerti Guru
Kelas 10 SMA Pendidikan Agama Hindu dan Budi Pekerti Guru
Kelas 10 SMA Pendidikan Agama Konghuchu dan Budi Pekerti Guru
Kelas 10 SMA Bahasa Indonesia Guru
Kelas 10 SMA Pendidikan Agama Buddha dan Budi Pekerti Guru
Kelas 10 SMA Prakarya dan Kewirausahaan Guru
Kelas 10 SMA Sejarah Indonesia Guru
Kelas 10 SMA Pendidikan Agama Kristen dan Budi Pekerti Guru
Kelas 10 SMA Matematika Guru
Kelas 10 SMA Pendidikan Agama Islam dan Budi Pekerti Guru
Kelas 10 SMA Penjaskes Guru
Kelas 10 SMA Bahasa Inggris Guru
Buku Siswa
Kelas 10 SMA Pendidikan Agama Kristen dan Budi Pekerti SiswaKelas 10 SMA Sejarah Indonesia Siswa
Kelas 10 SMA Bahasa Indonesia Siswa
Kelas 10 SMA Seni Budaya Siswa
Kelas 10 SMA Prakarya dan Kewirausahaan Siswa
Kelas 10 SMA Matematika Siswa Semester 1
Kelas 10 SMA Matematika Siswa Semester 2
Kelas 10 SMA Pendidikan Agama Konghuchu dan Budi Pekerti Siswa
Kelas 10 SMA Pendidikan Agama Katolik dan Budi Pekerti Siswa
Kelas 10 SMA Penjaskes Siswa
Kelas 10 SMA Bahasa Inggris Siswa
Kelas 10 SMA Pendidikan Agama Islam dan Budi Pekerti Siswa
Kelas 10 SMA Pendidikan Agama Buddha dan Budi Pekerti Siswa
Kelas 10 SMA Pendidikan Agama Hindu dan Budi Pekerti Siswa
Ikatan Kovalen
Ikatan Kovalen Adalah adanya pemakaian secara bersama elektron yang berikatan oleh dua atom.
Jenis Ikatan kovalen berdasarkan jumlah pasangan elektron yang berikatan di bagi atas tiga:
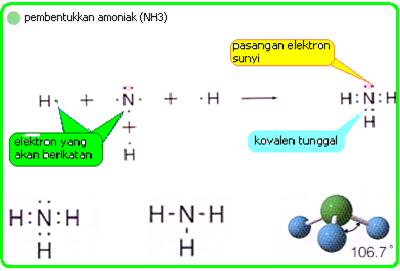
1. ikatan kovalen tunggal
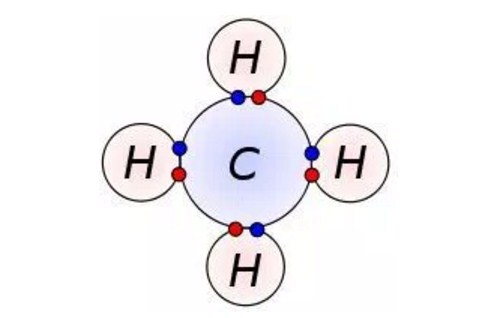
Adanya pemakaian satu pasang elektron oleh dua atom, misalnya adalah NH3, CH4. H2O.
Amoniak,Metana dan air: tiga contoh ikatan kovalen tunggal 2. ikatan kovalen rangkap dua
Ikatan ini melibatkan dua pasang elektron yang diguanakan secara bersama-sama. Contoh senyawa ikatan kovalen rangkap dua adalah O2 dan CO2.
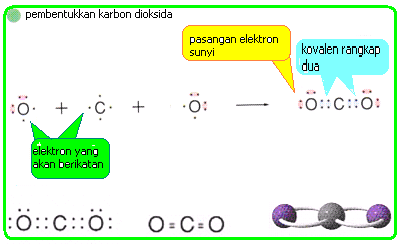
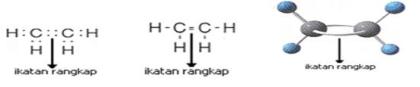
3. ikatan kovalen rangkap tiga
Ikatan ini melibatkan tiga pasang elektron yang digunakan secara bersama-sama. Contoh senyawa kovalen rangkap tiga adalah N2 dan C2H2.
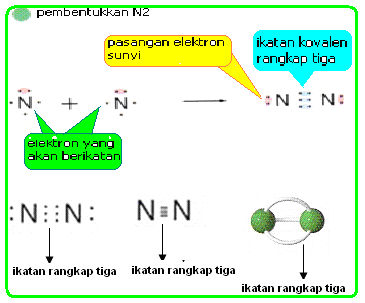
1. ikatan kovalen tunggal
Adanya pemakaian satu pasang elektron oleh dua atom, misalnya adalah NH3, CH4. H2O.
Amoniak,Metana dan air: tiga contoh ikatan kovalen tunggal 2. ikatan kovalen rangkap dua
Ikatan ini melibatkan dua pasang elektron yang diguanakan secara bersama-sama. Contoh senyawa ikatan kovalen rangkap dua adalah O2 dan CO2.


3. ikatan kovalen rangkap tiga
Ikatan ini melibatkan tiga pasang elektron yang digunakan secara bersama-sama. Contoh senyawa kovalen rangkap tiga adalah N2 dan C2H2.

Ikatan Kovalen Polar dan Non Polar
Ikatan kovalen polar
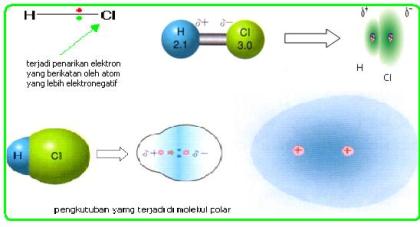
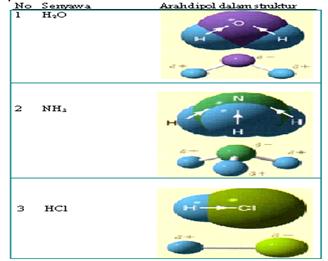
Ikatan kovalen polar adalah suatu ikatan kovalen dimana elektron-elektron yang membentuk ikatan lebih banyak menghabiskan waktunya untuk berputar dan berkeliling disekitar salah satu atom. Pada molekul HCl elektron yang berikatan akan lebih dekat kepada atom klor daripada Hidrogen. Polaritas ikatan ini dapat digambarkan dalam bentuk panah atau symbol δ+ , δ-. δ+ adalah tanda bahwa atom lebih bersifat elektropositif di banding dengan atom yang menjadi pasangannya. δ- berarti bahaw atom lebih bersifat elektronegatif daripada atom yang menjadi pasangan ikatannya. Lihat harga kelektronegtaifan tiap unsur pada tabel pauling
Ikatan kovalen nonpolar
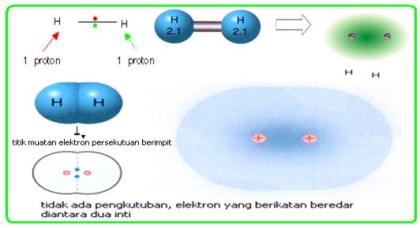
Kovalen murni (non polar) adalah memiliki ciri Titik muatan negatif elektron persekutuan berhimpit, sehingga pada molekul pembentukuya tidak terjadi momen dipol, dengan perkataan lain bahwa elektron persekutuan mendapat gaya tarik yang sama
Struktur H2 dan CO2 adalah contoh ikatan kimia non polar karena daya tariknya seimbang baik antara H dengan H atau antar O dengan C kiri dan kanan seimbang. Sehingga momen dipolnya menjadi nol Contoh lain adalah senyawa CH4, H2, O2, Br2 dan lain-lain
Ikatan kovalen polar adalah suatu ikatan kovalen dimana elektron-elektron yang membentuk ikatan lebih banyak menghabiskan waktunya untuk berputar dan berkeliling disekitar salah satu atom. Pada molekul HCl elektron yang berikatan akan lebih dekat kepada atom klor daripada Hidrogen. Polaritas ikatan ini dapat digambarkan dalam bentuk panah atau symbol δ+ , δ-. δ+ adalah tanda bahwa atom lebih bersifat elektropositif di banding dengan atom yang menjadi pasangannya. δ- berarti bahaw atom lebih bersifat elektronegatif daripada atom yang menjadi pasangan ikatannya. Lihat harga kelektronegtaifan tiap unsur pada tabel pauling
Ikatan kovalen nonpolar
Kovalen murni (non polar) adalah memiliki ciri Titik muatan negatif elektron persekutuan berhimpit, sehingga pada molekul pembentukuya tidak terjadi momen dipol, dengan perkataan lain bahwa elektron persekutuan mendapat gaya tarik yang sama
Struktur H2 dan CO2 adalah contoh ikatan kimia non polar karena daya tariknya seimbang baik antara H dengan H atau antar O dengan C kiri dan kanan seimbang. Sehingga momen dipolnya menjadi nol Contoh lain adalah senyawa CH4, H2, O2, Br2 dan lain-lain
Mengidentifikasi Keberadaan Ikatan Kovalen Koordinat pada Suatu Molekul
Bahasan struktur Lewis suatu molekul bagi sebagian siswa bukanlah
perkara mudah. Apalagi bila ilustrasi elektron yang diberikan tanpa
pembeda baik tanda atau warna. Namun demikian masih ada jalan lain yang
dapat digunakan untuk mengidentifikasi ikatan kovalen manakah yang
bertindak sebagai ikatan kovalen koordinat. Oh ya yang dimaksud dengan
ikatan kovalen adalah ikatan antara 2 atom yang menggunakan elektron
untuk digunakan secara bersama-sama dalam suatu molekul. Bila asal
elektron yang digunakan secara bersama-sama itu berasal dari salah satu
atom saja dari 2 atom disebut dengan ikatan kovalen koordinat. Bagaimana
cara mengetahui bahwa suatu ikatan kovalen itu berikatan kovalen biasa
atau berikatan kovalen koordinat?

Berikut langkah-langkahnya:
A. CO
Σ Elektron valensi C = 4; Σ ikatan sekitar C = 3; Σ elektron tak berikatan pada C = 2
Muatan formal C = 4 - 3 - 2 = -1
Σ Elektron valensi O = 6; Σ ikatan sekitar O = 3; Σ elektron tak berikatan pada O = 2
Muatan formal H = 6 - 3 - 2 = +1
B. CO2
Σ Elektron valensi C = 4; Σ ikatan sekitar C = 4; Σ elektron tak berikatan pada C = 0
Muatan formal C = 4 - 4 - 0 = 0
Σ Elektron valensi O = 6; Σ ikatan sekitar O = 2; Σ elektron tak berikatan pada O = 4
Muatan formal H = 6 - 2 - 4 = 0
C. HNO3
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi N = 6; Σ ikatan sekitar N = 4; Σ elektron tak berikatan pada N = 0
Muatan formal N = 5 - 4 - 0 = +1
Σ Elektron valensi Oa = 6; Σ ikatan sekitar Oa = 2; Σ elektron tak berikatan pada Oa = 4
Muatan formal Oa = 6 - 2 - 4 = 0
Σ Elektron valensi Ob = 6; Σ ikatan sekitar Ob = 2; Σ elektron tak berikatan pada Ob = 4
Muatan formal Ob = 6 - 2 - 4 = 0
Σ Elektron valensi Oc = 6; Σ ikatan sekitar Oc = 1; Σ elektron tak berikatan pada Oc = 6
Muatan formal Oc = 6 - 1 - 6 = -1
D. H2SO4
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi S = 6; Σ ikatan sekitar S = 4; Σ elektron tak berikatan pada S = 0
Muatan formal S = 6 - 4 - 0 = +2
Σ Elektron valensi Oa = 6; Σ ikatan sekitar Oa = 2; Σ elektron tak berikatan pada Oa = 4
Muatan formal Oa = 6 - 2 - 4 = 0
Σ Elektron valensi Ob = 6; Σ ikatan sekitar Ob = 1; Σ elektron tak berikatan pada Ob = 6
Muatan formal Ob = 6 - 1 - 6 = -1
Pada struktur H2SO4 gambar nomor 2, atom S
berikatan dengan 4 atom O yang terdiri 2 ikatan kovalen koordinasi
(ditandai dengan panah penghubung dari S menuju O) dan 2 ikatan kovalen
biasa.
Pada struktur H2SO4 gambar nomor 3 adalah struktur H2SO4 paling stabil karena muatan formal setiap atom adalah 0. Pada atom S memang tidak mengikuti kaidah oktet, hal ini boleh-boleh saja karena S termasuk unsur yang menempati periode 3 (memiliki 3 kulit) yang berarti memungkinkan untuk memiliki jumlah elektron di sekitarnya melebihi aturan oktet.
E. H2O
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi O = 6; Σ ikatan sekitar O = 2; Σ elektron tak berikatan pada O = 4
Muatan formal H = 6 - 2 - 4 = 0
F. NH3BF3
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi N = 5; Σ ikatan sekitar N = 4; Σ elektron tak berikatan pada N = 0
Muatan formal N = 5 - 4 - 0 = +1
Σ Elektron valensi B = 3; Σ ikatan sekitar B = 4; Σ elektron tak berikatan pada B = 0
Muatan formal H = 3 - 4 - 0 = -1
Σ Elektron valensi F = 7; Σ ikatan sekitar F = 1; Σ elektron tak berikatan pada F = 6
Muatan formal F = 7 - 1 - 6 = 0
Koreksi dan saran atas tulisan ini akan sangat bermanfaat untuk perbaikan sehingga tidak menyesatkan pembelajar kimia.
Terima kasih.
Berikut langkah-langkahnya:
A. CO
Σ Elektron valensi C = 4; Σ ikatan sekitar C = 3; Σ elektron tak berikatan pada C = 2
Muatan formal C = 4 - 3 - 2 = -1
Σ Elektron valensi O = 6; Σ ikatan sekitar O = 3; Σ elektron tak berikatan pada O = 2
Muatan formal H = 6 - 3 - 2 = +1
B. CO2
Σ Elektron valensi C = 4; Σ ikatan sekitar C = 4; Σ elektron tak berikatan pada C = 0
Muatan formal C = 4 - 4 - 0 = 0
Σ Elektron valensi O = 6; Σ ikatan sekitar O = 2; Σ elektron tak berikatan pada O = 4
Muatan formal H = 6 - 2 - 4 = 0
C. HNO3
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi N = 6; Σ ikatan sekitar N = 4; Σ elektron tak berikatan pada N = 0
Muatan formal N = 5 - 4 - 0 = +1
Σ Elektron valensi Oa = 6; Σ ikatan sekitar Oa = 2; Σ elektron tak berikatan pada Oa = 4
Muatan formal Oa = 6 - 2 - 4 = 0
Σ Elektron valensi Ob = 6; Σ ikatan sekitar Ob = 2; Σ elektron tak berikatan pada Ob = 4
Muatan formal Ob = 6 - 2 - 4 = 0
Σ Elektron valensi Oc = 6; Σ ikatan sekitar Oc = 1; Σ elektron tak berikatan pada Oc = 6
Muatan formal Oc = 6 - 1 - 6 = -1
D. H2SO4
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi S = 6; Σ ikatan sekitar S = 4; Σ elektron tak berikatan pada S = 0
Muatan formal S = 6 - 4 - 0 = +2
Σ Elektron valensi Oa = 6; Σ ikatan sekitar Oa = 2; Σ elektron tak berikatan pada Oa = 4
Muatan formal Oa = 6 - 2 - 4 = 0
Σ Elektron valensi Ob = 6; Σ ikatan sekitar Ob = 1; Σ elektron tak berikatan pada Ob = 6
Muatan formal Ob = 6 - 1 - 6 = -1
Pada struktur H2SO4 gambar nomor 2, atom S
berikatan dengan 4 atom O yang terdiri 2 ikatan kovalen koordinasi
(ditandai dengan panah penghubung dari S menuju O) dan 2 ikatan kovalen
biasa.
Pada struktur H2SO4 gambar nomor 3 adalah struktur H2SO4 paling stabil karena muatan formal setiap atom adalah 0. Pada atom S memang tidak mengikuti kaidah oktet, hal ini boleh-boleh saja karena S termasuk unsur yang menempati periode 3 (memiliki 3 kulit) yang berarti memungkinkan untuk memiliki jumlah elektron di sekitarnya melebihi aturan oktet.
E. H2O
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi O = 6; Σ ikatan sekitar O = 2; Σ elektron tak berikatan pada O = 4
Muatan formal H = 6 - 2 - 4 = 0
F. NH3BF3
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi N = 5; Σ ikatan sekitar N = 4; Σ elektron tak berikatan pada N = 0
Muatan formal N = 5 - 4 - 0 = +1
Σ Elektron valensi B = 3; Σ ikatan sekitar B = 4; Σ elektron tak berikatan pada B = 0
Muatan formal H = 3 - 4 - 0 = -1
Σ Elektron valensi F = 7; Σ ikatan sekitar F = 1; Σ elektron tak berikatan pada F = 6
Muatan formal F = 7 - 1 - 6 = 0
Koreksi dan saran atas tulisan ini akan sangat bermanfaat untuk perbaikan sehingga tidak menyesatkan pembelajar kimia.
Terima kasih.
Berikut langkah-langkahnya:
- Gambar struktur Lewis molekul (cara menggambar struktur Lewis silakan baca di sini atau ikuti petunjuk pada video dari youtube ini)
- Hitung muatan formal setiap atom dalam molekul.
Rumus hitung:
muatan formal atom = Σ e. valensi - Σ ikatan di sekitar atom - Σ elektron tak berikatan - Bila terdapat atom dengan muatan formal + (positif) dan atom lain yang berdekatan bernilai - (negatif) maka ikatan di antara kedua atom atom tersebut merupakan ikatan kovalen koordinat. Arahnya dari atom bermuatan formal + ke atom bermuatan formal -.
- Ikatan kovalen koordinat biasanya dimulai dari atom dengan muatan formal + menuju ke atom dengan muatan formal negatif.
A. CO
Σ Elektron valensi C = 4; Σ ikatan sekitar C = 3; Σ elektron tak berikatan pada C = 2
Muatan formal C = 4 - 3 - 2 = -1
Σ Elektron valensi O = 6; Σ ikatan sekitar O = 3; Σ elektron tak berikatan pada O = 2
Muatan formal H = 6 - 3 - 2 = +1
B. CO2
Σ Elektron valensi C = 4; Σ ikatan sekitar C = 4; Σ elektron tak berikatan pada C = 0
Muatan formal C = 4 - 4 - 0 = 0
Σ Elektron valensi O = 6; Σ ikatan sekitar O = 2; Σ elektron tak berikatan pada O = 4
Muatan formal H = 6 - 2 - 4 = 0
C. HNO3
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi N = 6; Σ ikatan sekitar N = 4; Σ elektron tak berikatan pada N = 0
Muatan formal N = 5 - 4 - 0 = +1
Σ Elektron valensi Oa = 6; Σ ikatan sekitar Oa = 2; Σ elektron tak berikatan pada Oa = 4
Muatan formal Oa = 6 - 2 - 4 = 0
Σ Elektron valensi Ob = 6; Σ ikatan sekitar Ob = 2; Σ elektron tak berikatan pada Ob = 4
Muatan formal Ob = 6 - 2 - 4 = 0
Σ Elektron valensi Oc = 6; Σ ikatan sekitar Oc = 1; Σ elektron tak berikatan pada Oc = 6
Muatan formal Oc = 6 - 1 - 6 = -1
D. H2SO4
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi S = 6; Σ ikatan sekitar S = 4; Σ elektron tak berikatan pada S = 0
Muatan formal S = 6 - 4 - 0 = +2
Σ Elektron valensi Oa = 6; Σ ikatan sekitar Oa = 2; Σ elektron tak berikatan pada Oa = 4
Muatan formal Oa = 6 - 2 - 4 = 0
Σ Elektron valensi Ob = 6; Σ ikatan sekitar Ob = 1; Σ elektron tak berikatan pada Ob = 6
Muatan formal Ob = 6 - 1 - 6 = -1
Pada struktur H2SO4 gambar nomor 3 adalah struktur H2SO4 paling stabil karena muatan formal setiap atom adalah 0. Pada atom S memang tidak mengikuti kaidah oktet, hal ini boleh-boleh saja karena S termasuk unsur yang menempati periode 3 (memiliki 3 kulit) yang berarti memungkinkan untuk memiliki jumlah elektron di sekitarnya melebihi aturan oktet.
E. H2O
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi O = 6; Σ ikatan sekitar O = 2; Σ elektron tak berikatan pada O = 4
Muatan formal H = 6 - 2 - 4 = 0
F. NH3BF3
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi N = 5; Σ ikatan sekitar N = 4; Σ elektron tak berikatan pada N = 0
Muatan formal N = 5 - 4 - 0 = +1
Σ Elektron valensi B = 3; Σ ikatan sekitar B = 4; Σ elektron tak berikatan pada B = 0
Muatan formal H = 3 - 4 - 0 = -1
Σ Elektron valensi F = 7; Σ ikatan sekitar F = 1; Σ elektron tak berikatan pada F = 6
Muatan formal F = 7 - 1 - 6 = 0
Koreksi dan saran atas tulisan ini akan sangat bermanfaat untuk perbaikan sehingga tidak menyesatkan pembelajar kimia.
Terima kasih.
Mengidentifikasi Keberadaan Ikatan Kovalen Koordinat pada Suatu Molekul
Kamis, 08 September 2016
Bahasan struktur Lewis suatu molekul bagi sebagian siswa bukanlah perkara mudah. Apalagi bila ilustrasi elektron yang diberikan tanpa pembeda baik tanda atau warna. Namun demikian masih ada jalan lain yang dapat digunakan untuk mengidentifikasi ikatan kovalen manakah yang bertindak sebagai ikatan kovalen koordinat. Oh ya yang dimaksud dengan ikatan kovalen adalah ikatan antara 2 atom yang menggunakan elektron untuk digunakan secara bersama-sama dalam suatu molekul. Bila asal elektron yang digunakan secara bersama-sama itu berasal dari salah satu atom saja dari 2 atom disebut dengan ikatan kovalen koordinat. Bagaimana cara mengetahui bahwa suatu ikatan kovalen itu berikatan kovalen biasa atau berikatan kovalen koordinat?Berikut langkah-langkahnya:
- Gambar struktur Lewis molekul (cara menggambar struktur Lewis silakan baca di sini atau ikuti petunjuk pada video dari youtube ini)
- Hitung muatan formal setiap atom dalam molekul.
Rumus hitung:
muatan formal atom = Σ e. valensi - Σ ikatan di sekitar atom - Σ elektron tak berikatan - Bila terdapat atom dengan muatan formal + (positif) dan atom lain yang berdekatan bernilai - (negatif) maka ikatan di antara kedua atom atom tersebut merupakan ikatan kovalen koordinat. Arahnya dari atom bermuatan formal + ke atom bermuatan formal -.
- Ikatan kovalen koordinat biasanya dimulai dari atom dengan muatan formal + menuju ke atom dengan muatan formal negatif.
A. CO
Σ Elektron valensi C = 4; Σ ikatan sekitar C = 3; Σ elektron tak berikatan pada C = 2
Muatan formal C = 4 - 3 - 2 = -1
Σ Elektron valensi O = 6; Σ ikatan sekitar O = 3; Σ elektron tak berikatan pada O = 2
Muatan formal H = 6 - 3 - 2 = +1
B. CO2
Σ Elektron valensi C = 4; Σ ikatan sekitar C = 4; Σ elektron tak berikatan pada C = 0
Muatan formal C = 4 - 4 - 0 = 0
Σ Elektron valensi O = 6; Σ ikatan sekitar O = 2; Σ elektron tak berikatan pada O = 4
Muatan formal H = 6 - 2 - 4 = 0
C. HNO3
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi N = 6; Σ ikatan sekitar N = 4; Σ elektron tak berikatan pada N = 0
Muatan formal N = 5 - 4 - 0 = +1
Σ Elektron valensi Oa = 6; Σ ikatan sekitar Oa = 2; Σ elektron tak berikatan pada Oa = 4
Muatan formal Oa = 6 - 2 - 4 = 0
Σ Elektron valensi Ob = 6; Σ ikatan sekitar Ob = 2; Σ elektron tak berikatan pada Ob = 4
Muatan formal Ob = 6 - 2 - 4 = 0
Σ Elektron valensi Oc = 6; Σ ikatan sekitar Oc = 1; Σ elektron tak berikatan pada Oc = 6
Muatan formal Oc = 6 - 1 - 6 = -1
D. H2SO4
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi S = 6; Σ ikatan sekitar S = 4; Σ elektron tak berikatan pada S = 0
Muatan formal S = 6 - 4 - 0 = +2
Σ Elektron valensi Oa = 6; Σ ikatan sekitar Oa = 2; Σ elektron tak berikatan pada Oa = 4
Muatan formal Oa = 6 - 2 - 4 = 0
Σ Elektron valensi Ob = 6; Σ ikatan sekitar Ob = 1; Σ elektron tak berikatan pada Ob = 6
Muatan formal Ob = 6 - 1 - 6 = -1
Pada struktur H2SO4 gambar nomor 3 adalah struktur H2SO4 paling stabil karena muatan formal setiap atom adalah 0. Pada atom S memang tidak mengikuti kaidah oktet, hal ini boleh-boleh saja karena S termasuk unsur yang menempati periode 3 (memiliki 3 kulit) yang berarti memungkinkan untuk memiliki jumlah elektron di sekitarnya melebihi aturan oktet.
E. H2O
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi O = 6; Σ ikatan sekitar O = 2; Σ elektron tak berikatan pada O = 4
Muatan formal H = 6 - 2 - 4 = 0
F. NH3BF3
Σ Elektron valensi H = 1; Σ ikatan sekitar H = 1; Σ elektron tak berikatan pada H = 0
Muatan formal H = 1 - 1 - 0 = 0
Σ Elektron valensi N = 5; Σ ikatan sekitar N = 4; Σ elektron tak berikatan pada N = 0
Muatan formal N = 5 - 4 - 0 = +1
Σ Elektron valensi B = 3; Σ ikatan sekitar B = 4; Σ elektron tak berikatan pada B = 0
Muatan formal H = 3 - 4 - 0 = -1
Σ Elektron valensi F = 7; Σ ikatan sekitar F = 1; Σ elektron tak berikatan pada F = 6
Muatan formal F = 7 - 1 - 6 = 0
Koreksi dan saran atas tulisan ini akan sangat bermanfaat untuk perbaikan sehingga tidak menyesatkan pembelajar kimia.
Terima kasih.